余宏杰课题组在新冠疫苗接种的全球多样性和Delta株所致疾病负担领域取得系列进展
近期,复旦大学余宏杰课题组在全球新冠疫苗接种的多样性和Delta变异株输入中国导致流行的疾病负担领域取得系列进展,2篇文章分别发表在BMC Medicine和Emerging Microbes & Infections。
一、全球新冠疫苗的接种政策、接种率和需求
自2020年12月始,全球陆续开展新冠疫苗的大规模接种,至今已逾一年多,各国在新冠疫苗的接种政策、进程和需求等方面的差异日渐凸显。从接种策略、使用的疫苗类型、接种率、需求等多个维度全方面了解各国新冠疫苗的接种现状,可为疫苗在全球范围内的公平分配、进一步提高接种率提供更全面的决策视角。为此,余宏杰课题组系统收集了各国的疫苗接种政策、接种量和目标人群等数据,全面刻画了各国新冠疫苗的接种类型、接种政策、接种率及其影响因素,以及未来完成目标人群接种的疫苗需求。研究结果以“Global diversity of policy, coverage, and demand of COVID-19 vaccines: a descriptive study”为题,于2022年4月4日在线发表在BMC Medicine(论文链接: https://bmcmedicine.biomedcentral.com/ articles/10.1186/s12916-022-02333-0)。
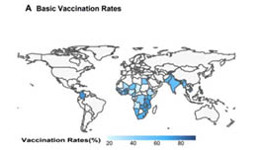
研究结果表明,腺病毒载体疫苗、mRNA疫苗、灭活疫苗、蛋白亚单位疫苗和结合疫苗分别在180、159、116、10和3个国家实施接种。在批准为一般人群接种疫苗的192个国家中,有32.3%的国家已将接种对象推广至5 岁及以上的儿童。48个国家和 151 个国家分别启动了额外基础免疫和加强免疫接种项目(图1)。全球平均每 100名目标人群中接种了 162.1 剂疫苗,但存在明显的区域和国家间的异质性。全人群疫苗接种率与医疗质量和可及性(HAQ)指数(R2 = 0.59)、社会人口学指数(SDI)(R2 = 0.52)和人均GDP(R2 = 0.61)均存在相关性。完成当前的目标人群接种至少仍需 64 亿剂次新冠疫苗,其中33 亿剂次用于基础免疫,31 亿剂次用于额外/加强免疫。

图1. 全球各国新冠疫苗基础免疫、额外接种和加强接种的目标人群。疫苗政策数据截止至2022年2月8日。
本研究定量刻画了全球各国新冠疫苗接种的政策、接种率和需求,揭示了现阶段疫苗接种的不公平和不均衡性,提示部分国家的低接种率可能会阻碍对新冠大流行的控制。奥密克戎变异株的出现更加凸显了填补全球疫苗接种鸿沟的重要性。本研究呼吁更多的国家和非政府组织参与到推动全球新冠疫苗接种的合作行动中,共同克服财政、政治和技术上的挑战,实现更加均衡和公平的疫苗接种。
复旦大学公共卫生学院2020级硕士生陈志元、2019级直博生郑雯、2020级博士生吴谦惠、2019级硕士生陈星会和2020级博士生彭珵为共同第一作者,复旦大学公共卫生学院教授、上海市重大传染病和生物安全研究院和复旦大学附属华山医院感染病科双聘PI余宏杰为通讯作者。
二、新冠病毒Delta变异株输入中国导致流行的疾病负担
新冠病毒(SARS-CoV-2)Delta变异株于2020年10月在印度发现。相较于原型株,Delta变异株有更高的传播力和毒力,且免疫逃逸能力增强。2021年6-12月,Delta变异株成为绝对优势毒株,随后与Omicron变异株共同循环,在全球引起了多轮流行高峰。接种新冠疫苗可有效降低重症发生风险。由于多数国家采取按年龄由高到低的优先接种顺序,老人疫苗接种率较高。自Delta变异株广泛传播后,较多国家观察到儿童新冠肺炎发病和住院比例呈明显上升趋势。
我国成功控制2020年初的武汉疫情后,持续面临由境外输入引发本土暴发流行的风险,陆续出现了多起由输入Delta变异株导致的本土疫情。在采取大规模核酸检测、旅行限制等非药物干预措施以遏制疫情的同时,我国通过大规模接种新冠疫苗加速构筑免疫屏障,于2021年7月将接种人群由成人扩大到12-17岁青少年,10月底进一步扩大到3-11岁儿童。此时,≥12岁和3-11岁人群接种率约为92%和1%。然而,现有基于新冠病毒原型株开发的灭活疫苗针对变异株感染的保护效果较原型株存在一定程度的下降。鉴于儿童的接种率低于成人,一旦发生境外输入Delta变异株引起本土疫情暴发、流行,其疾病负担如何?是否会向儿童倾斜?亟需回答此关键科学问题,为适时调整和优化新冠肺炎防控策略提供科学证据。
为此,余宏杰课题组构建了随机易感-感染-恢复(SIR)传播动力学模型,基于我国人口学特征、人群接触模式、Delta变异株基本再生数和毒力、疫苗接种现状以及针对变异株的疫苗保护效果等关键参数,估计了潜在Delta变异株输入引起流行后半年内所导致的疾病负担,以及当前疫苗接种策略对疾病负担的影响。研究结果以“Assessing the transition of COVID-19 burden towards the young population while vaccines are rolled out in China”为题,于4月25日以研究长文(Research Article)的形式在线发表在Emerging Microbes & Infections(论文链接:https://www.tandfonline.com/doi/full/10.1080/22221751.2022. 2063073)。
模型基线情境假设2021年12月1日境外输入40例Delta变异株感染病例。根据我国新冠疫苗免疫策略和接种率数据,本研究模拟了:(1)“成人+青少年”接种策略,即随机接种≥12岁人群,排除孕妇、疫苗接种禁忌症者和既往感染者。Delta变异株引入时,≥12岁人群接种率为92.5%。(2)“成人+青少年+儿童”接种策略,即自2021年10月28日起,接种人群扩大到3-11岁(占全人口的11%)。Delta变异株引入时,≥12岁和3-11岁接种率分别为92.5%和43.9%。
在“成人+青少年”接种策略下,Delta变异株流行所致全人群有症状病例、住院、入住ICU和死亡的发生率分别为439/1000(95%CI:415-447/1000),27/1000(25-28/1000),5.4/1000(5.2-5.6/1000)和2.4/1000(2.2-2.5/1000),是2020年春武汉疫情所致疾病负担的7-55倍(图2)。其中,11.2%的有症状病例和5.1%住院发生在<12岁儿童。
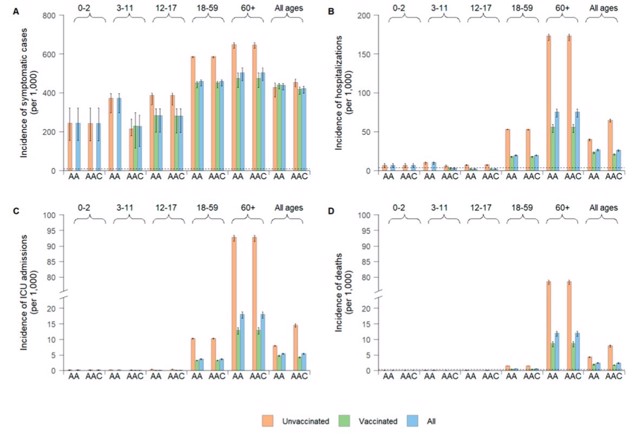
图2. 新冠病毒Delta变异株在国内流行半年所致疾病负担
(A)有症状病例发生率;(B)住院率;(C)入住ICU发生率;(D)死亡率。(A)、(B)和(D)中水平虚线表示2020年春武汉疫情所致相应的疾病负担。AA:“成人+青少年”接种策略;AAC:“成人+青少年+儿童” 接种策略
与之相比,“成人+青少年+儿童”接种策略将疫苗接种扩大到3-11岁人群,可明显降低该年龄组有症状感染(39%)和住院(68%),但并不足以阻断病毒传播,对其他年龄组疾病负担的影响很小(图2)。若疫苗接种不推广到3-11岁(反事实情境),0-2岁和3-11岁儿童中有症状感染的率比(指年龄别发病率与总人群发病率的比值)将分别增加15%和30%,住院患者的率比分别增加110%和137%(图3)。
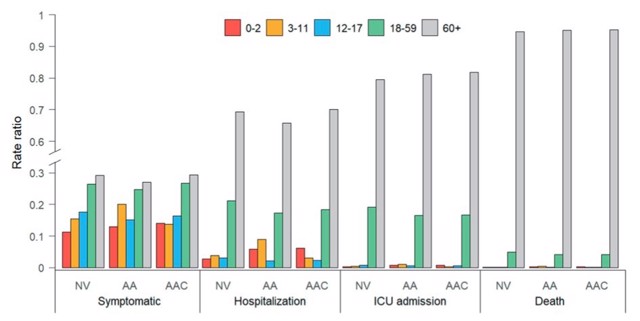
图3. Delta变异株有症状病例感染、住院、入住ICU和死亡的率比
NV:不接种疫苗;AA:“成人+青少年”接种策略;AAC:“成人+青少年+儿童”接种策略
无论哪种策略,接种疫苗均可降低发病和出现严重临床结局的风险。分年龄组来看,不接种疫苗人群有症状病例、住院、入住ICU和死亡的发生率分别是接种疫苗人群的0.9-1.4倍、2.0-3.1倍、2.1-3.3倍和2.1-3.3倍(图2)。
本研究进一步模拟了提高新冠疫苗保护效果以及采取非药物干预措施对疾病负担的影响。疫苗预防Delta变异株感染的保护效果越好,将疾病负担控制在较低水平所需采取的非药物干预措施的强度将越低,越有利于恢复正常的社会生活秩序。在“成人+青少年+儿童”接种策略下,当疫苗保护效果超过88%时,即使不采取任何非药物干预措施,也可将Delta变异株流行所致死亡人数控制在低于我国季节性流感流行每年所致超额呼吸系统疾病死亡的水平(88,100人)。
综上,考虑到Delta变异株更高的传播力和毒力,以及疫苗对其更低的保护效果,尽管我国≥12岁人群已有较高的疫苗覆盖率,但Delta变异株一旦在国内流行,仍将造成严重的疾病负担。研究结果支持我国将目标接种人群扩大至3-11岁,以避免疾病负担向该年龄段倾斜;并强调应继续维持一定强度的非药物干预措施,快速推进加强免疫,并积极研发保护效果更好的疫苗,以应对具有更高传播力、致病力和毒力的变异株流行。
复旦大学公卫学院博士后蔡俊和复旦大学公卫学院、上海市重大传染病和生物安全研究院的杨娟副教授是共同第一作者,复旦大学公卫学院教授、上海市重大传染病和生物安全研究院、复旦大学附属华山医院感染病科双聘PI余宏杰为通讯作者。
以上研究得到国家自然科学基金重点项目(82130093)、国家重点研发计划(2021YFC0863400)和上海市市级科技重大专项(ZD2021CY001)等项目的资助。