张蕴晖教授团队提出孤独症“微环境失调模型”为机制分型与精准干预提供新视角
(撰稿:赵迎亚)
复旦大学公共卫生学院张蕴晖教授、赵迎亚青年副研究员团队与复旦大学附属儿科医院合作,近期在《Med》(Cell Press旗下期刊,2026年4月刊封面特辑)发表长篇综述“Microenvironment dysregulation in autism spectrum disorder: Immune, epigenetic, synaptic, and gut-brain mechanisms”。该综述针对孤独症谱系障碍高度异质的临床与生物学特征,系统总结了免疫、表观遗传、突触功能及肠—脑轴等关键领域的研究进展,并在此基础上提出“微环境失调模型”。这一模型为揭示ASD的核心病理机制、识别可干预的生物学亚型,以及推动从机制到精准干预的转化研究提供了新思路。

ASD是一类常见且高度异质的儿童神经发育障碍疾病。近年来,围绕其遗传基础、环境影响及相关生物学机制的研究不断深入,但这些证据长期分散在不同研究方向中,整体上仍缺少一个相对统一的解释框架。张蕴晖教授团队认为,ASD并非由某一个单独因素所致,而更可能是在遗传易感背景下,多种生物学过程在发育关键阶段共同作用的结果。基于这一认识,文章提出“微环境失调模型”,认为遗传易感性与环境暴露可能在少数关键通路上发生交汇,并共同作用于中枢神经系统和外周胃肠道这两个重要生物学微环境。在这一模型下,生命早期免疫失衡在部分个体中可与遗传风险相互作用,进一步影响表观遗传程序、神经免疫信号、突触发育及肠脑轴稳态,最终参与ASD神经发育轨迹和行为表型的形成。这一模型并不是试图用单一路径解释所有ASD,而是希望在复杂差异中寻找具有共同基础的机制线索,为理解其复杂异质性提供一个更连贯的分析视角。
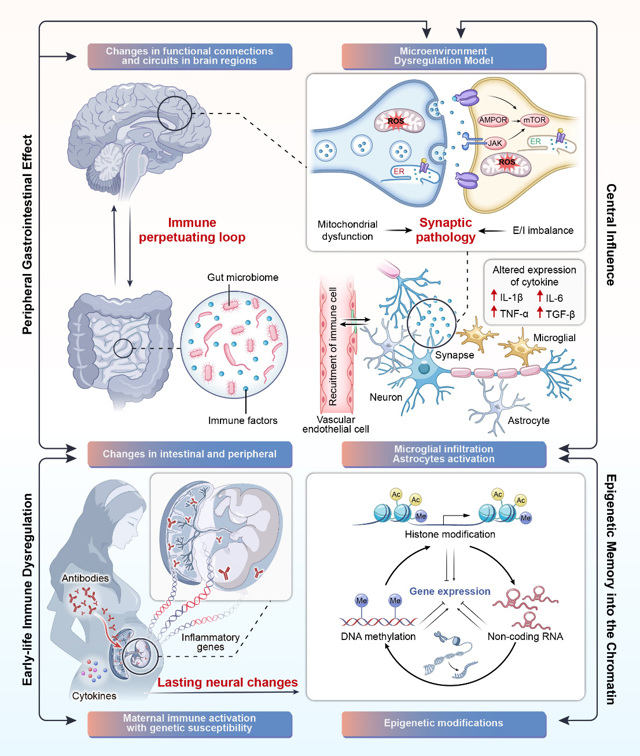
文章同时指出,该模型为后续相关研究指明了更为清晰的方向。一方面,有助于进一步精准识别不同生物学亚型,推动关键生物标志物的发掘与验证;另一方面,也为开展机制导向的干预研究提供了全新思路与实践切入点。团队认为未来ASD研究需要从单个危险因素的不断增加,进一步转向跨遗传、环境、脑和肠系统的纵向整合研究,更深入地描绘不同亚型的关键失调入口及其动态演变过程。
复旦大学公共卫生学院青年副研究员赵迎亚、复旦大学医学遗传研究院青年研究员袁博和复旦大学附属儿科医院副研究员马文娟为文章的共同第一作者,复旦大学附属儿科医院王艺教授、复旦大学公共卫生学院张蕴晖教授和复旦大学脑转化研究院彭勃教授为文章的共同通讯作者。
原文链接:https://www.sciencedirect.com/science/article/abs/pii/S2666634026000371